Ο FDA δίνει το πράσινο φως στην πρώτη συσκευή παρακολούθησης γλυκόζης που χορηγείται χωρίς ιατρική συνταγή.
O Οργανισμός Τροφίμων και Φαρμάκων των ΗΠΑ (FDA) ενέκρινε τη διάθεση στην αγορά του πρώτου μη συνταγογραφούμενου (OTC) συστήματος συνεχούς παρακολούθησης γλυκόζης (CGM). Το Dexcom Stelo Glucose Biosensor System είναι ένα ολοκληρωμένο CGM (iCGM) που προορίζεται για οποιονδήποτε 18 ετών και άνω που δεν χρησιμοποιεί ινσουλίνη, όπως άτομα με διαβήτη που αντιμετωπίζουν την κατάστασή τους με από του στόματος φάρμακα ή άτομα χωρίς διαβήτη που θέλουν να κατανοήσουν καλύτερα τον τρόπο διατροφής και Η άσκηση μπορεί να επηρεάσει τα επίπεδα σακχάρου στο αίμα. Είναι σημαντικό ότι αυτό το σύστημα δεν είναι για άτομα με προβληματική υπογλυκαιμία (χαμηλό σάκχαρο αίματος), καθώς το σύστημα δεν έχει σχεδιαστεί για να ειδοποιεί τον χρήστη για αυτήν την δυνητικά επικίνδυνη κατάσταση.
«Τα CGM μπορούν να είναι ένα ισχυρό εργαλείο για την παρακολούθηση της γλυκόζης στο αίμα. Η σημερινή άδεια επεκτείνει την πρόσβαση σε αυτές τις συσκευές επιτρέποντας σε άτομα να αγοράσουν ένα CGM χωρίς τη συμμετοχή παρόχου υγειονομικής περίθαλψης», δήλωσε ο Jeff Shuren, MD, JD, διευθυντής του Κέντρου Συσκευών και Ακτινολογικής Υγείας του FDA. «Η παροχή σε περισσότερα άτομα πολύτιμων πληροφοριών σχετικά με την υγεία τους, ανεξάρτητα από την πρόσβασή τους σε γιατρό ή ασφάλιση υγείας, είναι ένα σημαντικό βήμα προς τα εμπρός για την προώθηση της ισότητας υγείας για τους ασθενείς των ΗΠΑ».
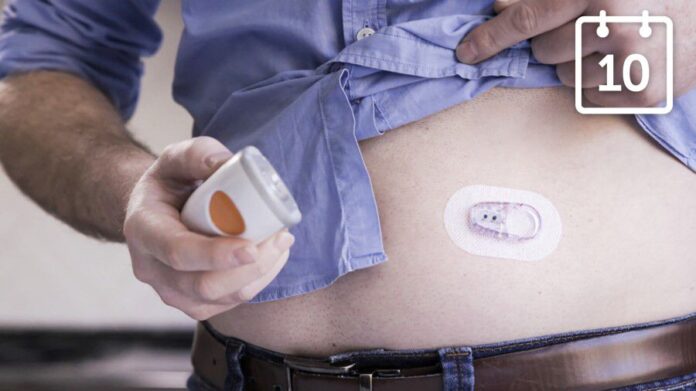
Το Stelo Glucose Biosensor System χρησιμοποιεί έναν φορετό αισθητήρα, σε συνδυασμό με μια εφαρμογή εγκατεστημένη στο smartphone ή σε άλλη έξυπνη συσκευή του χρήστη, για τη συνεχή μέτρηση, καταγραφή, ανάλυση και εμφάνιση τιμών γλυκόζης σε άτομα 18 ετών και άνω που δεν λαμβάνουν ινσουλίνη και δεν λαμβάνουν έχουν προβληματική υπογλυκαιμία. Οι χρήστες μπορούν να φορούν κάθε αισθητήρα έως και 15 ημέρες πριν τον αντικαταστήσουν με νέο αισθητήρα. Η συσκευή παρουσιάζει μετρήσεις γλυκόζης αίματος και τάσεις κάθε 15 λεπτά στη συνοδευτική εφαρμογή. Οι χρήστες δεν πρέπει να λαμβάνουν ιατρικές αποφάσεις με βάση την έξοδο της συσκευής χωρίς να μιλήσουν με τον πάροχο υγειονομικής περίθαλψης.
Τα δεδομένα από μια κλινική μελέτη που παρασχέθηκε στον FDA έδειξαν ότι η συσκευή είχε παρόμοια απόδοση με άλλα iCGM. Οι ανεπιθύμητες ενέργειες που αναφέρθηκαν στη μελέτη περιελάμβαναν τοπική μόλυνση, ερεθισμό του δέρματος και πόνο ή δυσφορία.


 Ακολουθήστε το Cibum
Ακολουθήστε το Cibum 













